什么是稳定同位素?
由于原子核所含有的中子数不同,具有相同质子数的原子具有不同的质量,这些原子被称为同位素。例如,碳的3个主要同位素分别为12C、13C和14C,它们都有6个质子和六个电子,但中子数则分别为6、7和8。与质子相比,含有太多或太少中子均会导致同位素的不稳定性,如14C。这些不稳定的“放射性同位素”将会衰变成稳定同位素。而12C和13C则因为质子和中子所特有的稳定结合,不发生衰变,即为稳定同位素。
稳定同位素含量如何测量?
在生态学和环境科学研究中最常用的是碳、氮、硫、氧和氢的稳定同位素,这些稳定性同位素可以通过气体同位素比率质谱分析法测得。首先将样品转化成气体(如CO2,N2,SO2或H2),在离子源中将气体分子离子化(从每个分子中剥离一个电子,导致每个分子带有一个正电荷),接着将离子化气体打入飞行管中。飞行管是弯曲的,磁铁置于其上方,带电分子依质量不同而分离,含有重同位素的分子弯曲程度小于含轻同位素的分子。在飞行管的末端有一个法拉第收集器,用以测量经过磁体分离之后,具有特定质量的离子束强度。
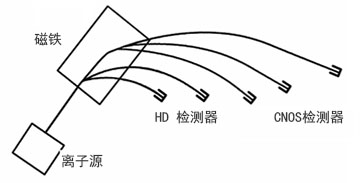
以CO2为例,需要有三个法拉第收集器来收集质量分别为44、45和46的离子束。不同质量离子同时收集,从而可以精确测定不同质量离子之间的比率。
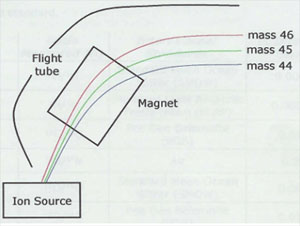
图 CO2的三个最常见质量——44(12C,16O,16O)、45(13C,16O,16O)和46(12C,18O,16O)在质谱仪飞行管中的分布图。进入飞行管的CO2在通过离子源时,每个分子都被剥离一个电子,形成带正电的离子。在飞行管中,磁场导致离子发生偏离,偏离半径与离子的质量/电荷比率成比例。重离子比轻离子偏离小(偏离半径大)。以CO2为例,质量为46的离子偏离半径最大,质量为44的离子偏离半径最小,质量为45的离子则介于两者之间。电荷也会影响偏离半径,但对于绝大多数分子而言,由于离子源仅剥离一个电子,因此,离子电荷数基本是恒定的。
在稳定同位素地球化学和生态学研究中,人们感兴趣的是物质同位素组成的微小变化,而不是绝对值的大小,同时为了便于进行比较,物质的同位素组成除了用同位素比率R表示外,更常用同位素比值(δ值,简读为“delta”值)表示(McKinney et al.,1950),其定义为:
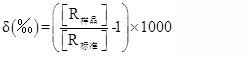
它表示了样品中两种同位素比值相对于某一标准对应比值的相对千分差。当δ值大于零时,表示样品的重同位素比标准物富集(enrichment),小于零时则比标准物贫化(depletion)。因此,δ值能清晰地反映同位素组成的变化。实际应用中,δ值就是物质同位素组成的代名词,例如13C、D、18O、15N、34S分别表示碳、氢、氧、氮和硫稳定同位素相对于各自标准物的比值。以碳同位素为例,AT%、13C/12C值与13C值可以根据下式转换:
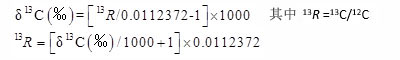
式中,0.0112372为碳同位素测试标准物的R值(表1-2)。因此,
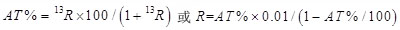
由于样品的δ值总是相对于某个标准物而言的,因而同一物质比较的标准物不同,得出的δ值也各异。因此,对样品间稳定同位素组成进行对比时必须采用同一标准物,或者将各实验室的数据换算成国际公认的统一标准。一个好的标准物应该满足以下要求:①同位素组成均一,大致为天然同位素组成变化范围的中间值;②数量大,以供长期使用和③化学制备和同位素测试操作较容易。目前普遍使用的国际公认标准物包括SMOW、 PDB、CDT和N2-atm等。
| 元素 | δ符号 | 测量比率(R) | 国际标准 | R, 国际标准 |
| H | δD | 2H/1H 2H/1H |
标准平均海水 (SMOW) 标准南极轻降水(SLAP) |
R0.00015575 0.000089089 |
| C | δ13C δ13C |
13C/12C 13C/12C |
Pee Dee Belemnite (PDB) Vienna-Pee Dee Belemnite(V-PDB) |
0.0112372 0.01111797 |
| N | δ15N | 15N/14N | 大气 | 0.003676 |
| O | δ18O | 18O/16O 18O/16O 18O/16O |
标准平均海水 (SMOW) Pee Dee Belemnite (PDB) 标准南极轻降水(SLAP) |
0.0020052 0.0020672 0.0018939 |
| S | δ34S | 34S/32S | Canyon Diablo Triolite(CDT) | 0.045005 |
如何在生态和环境科学研究中运用稳定同位素?
稳定同位素技术的出现加深了生态学家对生态系统过程的进一步了解,使生态学家可以探讨一些其它方法无法研究的问题。正如现代分子生物技术大大地推动了基因、生物化学和进化生物学的研究一样,稳定同位素技术对生态学研究也已产生了重要的影响。通过使用稳定性同位素技术,可以使生态学家测出许多随时空变化的生态过程,同时又不会对生态系统的自然状态和元素的性质造成干扰。在过去的十几年中,一些生态与环境科学的最令人瞩目的进步依赖于稳定性同位素技术,稳定性同位素能够被用来解决生态与环境科学的许多问题。包括:
- 植物如何有效地利用水分(13C)?
- 植物从土壤哪个层次获得水分(18O, 2H)?
- 植物通过氮固定或吸收土壤NH4+及NO3-获得氮素比例(15N)?
- 如何确定土壤中碳和氮周转速率(13C, 15N)?
- 区分土壤呼吸释放CO2的来源(植物根系或土壤微生物)(13C, 18O)。
- 区分光合和呼吸对净生态系统CO2交换或NEE的相对贡(13C, 18O)。
- 区分蒸腾和蒸发对净生态系统水交换或蒸散(ET)的相对贡(2H, 18O)。
- 如何判定N2O的来源(硝化细菌或反硝化细菌)(15N, 18O)?
- 确定食物网初级消费者事物来源(13C, 34S)。
- 确定食物链的长度(15N)。
- 如何确定空气和水体污染物的来源(15N, 34S, 18O)。
- 确定城市能源消耗对大气CO2, CO和氮化物的贡献((13C , 15N, 18O)。
- 判断动物如候鸟、蝴蝶等的迁徙路线(18O, 2H)。
- 判定史前人类社会是否以谷物作为食物来源(13C)。
- 毒品、兴奋剂、爆炸物等违禁品的来源(15N, 18O, 2H,13C,34S)。
- 食品掺假检测、产品产地溯源(15N, 18O, 2H,13C, 34S)。
与其它技术相比,稳定同位素技术的优点在于使得这些生态和环境科学问题的研究能够定量化并且是在没有干扰(如没有放射性同位素的环境危害)的情况下进行。有些问题还只能通过利用稳定同位素技术来解决。例如,植物在光合作用倾向于吸收含有轻碳同位素(12C)的CO2,其吸收程度受有效水含量和光合途径影响,水分有效性和光合途径是干旱或湿润环境植物的重要特性。因此,植物13C组成能够在时间尺度上整合反映植物的水分利用效率。通过测量植物茎水2H和18O组成,也能够判定植物对表层水和深层水的依赖程度。另一方面,通过向土壤添加15NH4+,并监测14NH4+对其稀释速率,就能够测定独立于硝化和固持(NH4+消耗过程)之外的土壤有机物质的矿化速率。通过在原位添加富含15N的NH4+或NO3-,并监测土壤中15N和14N,就能够量化每种微生物转化量。